心血管病是人類健康的第一大殺手。據《中國心血管健康與疾病報告2021》推算,我國心血管病現患人數已達3.3億,並伴隨人口老齡化的進程快速上升。在新冠病毒大流行中,患有心血管基礎病的感染者俱有更高的重症率和死亡率,並且健康人群感染新冠後發生心血管病的風險也會激增。雖然現階段已經上市多種心血管病治療藥物,但它們時常存在明顯的副作用,所以心血管疾病新靶標的發現和新機制藥物的研發具有重要意義。

侯盼盼助理教授(右一)及課題組成員:嚴珍珍博士後(左一)、鍾玲研究助理(中)
2022年11月8日,澳科大中藥質量研究國家重點實驗室——埃爾文•內爾博士生物物理與創新藥物實驗室侯盼盼助理教授課題組與浙江大學基礎醫學院郭江濤教授和楊巍教授課題組在權威期刊美國國家科學院院刊PNAS上合作發表了題為“Structural mechanisms for the activation of human cardiac KCNQ1 channel by electro-mechanical coupling enhancers”的研究論文,侯盼盼助理教授為該論文的通訊作者。該研究結合冷凍電鏡與電生理技術,解析了人源KCNQ1-CaM複合體在apo狀態、小分子激動劑ML277結合狀態、以及ML277和膜磷脂PIP2同時結合狀態的4個高分辨率結構,並闡明了外源和內源性配體激活KCNQ1通道的分子機制,為KCNQ1通道做為抗心血管病新靶標的功能確證和藥物篩選奠定了基礎。
侯盼盼助理教授多年來一直專注KCNQ1通道的基礎與轉化研究(Nat. Commun. 2017, 2020; eLife. 2019, 2020)。 KCNQ 鉀通道家族(KCNQ1-KCNQ5)廣泛表達於人體的心臟、大腦和消化道等重要器官,是有潛力的治療心臟病、精神疾病和癌症的靶標。其中,KCNQ1通道大量表達於心臟,參與心肌動作電位的複極化過程,對控制心律至關重要。臨床研究已經發現KCNQ1通道的數百個功能缺失突變體都會引起長QT綜合症(LQT1,佔所有LQT病例的30-35%),導致心律失常和猝死。本研究為靶向調控KCNQ1通道進行心臟病的精準治療提供了新的思路。該研究受到澳門科學技術發展基金和國家自然科學基金的資助。
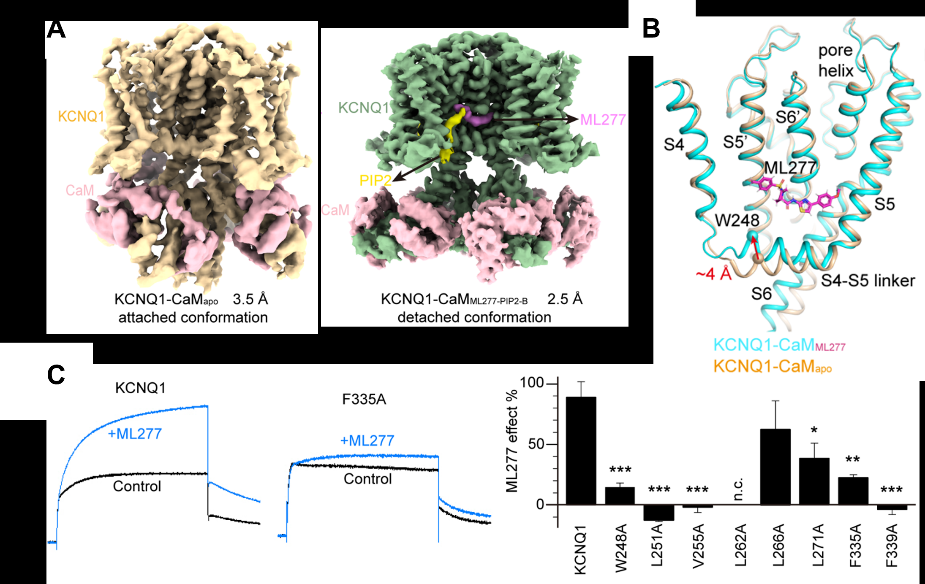
KCNQ1通道與外源小分子ML277和內源磷脂分子PIP2的高分辨率結構複合體。(A)KCNQ1-CaMApo和KCNQ1-CaMML277-PIP2-B高分辨率結構。(B)KCNQ1-CaMApo和KCNQ1-CaMML277結構對比以顯示ML277的結合位點和引起的通道構象變化:S4-S5 linker的N端(「肘部」位置)明顯上移。(C)Alanine突變與電生理驗證ML277的結合位點。





